产品介绍
本试剂盒可以快速从细胞、细菌和动物组织中提取总 RNA。本产品中裂解液(RLT Lysis Buffer) 可以快速裂解细胞和灭活 RNA 酶,通过 DNA 清除/RNA 吸附通用柱吸附技术,去除基因组 DNA 残留,同时在乙醇辅助结合条件下,高效地结合在吸附柱的硅胶膜上,再经过多次的洗涤离心后,去除细胞代谢物和蛋白质等杂质,获得纯净的总 RNA。纯化的 RNA 可用于 RT-PCR,Northern Blot,Poly(A)+筛选等多种实验。
产品特色
✔ 安全性高:不需要使用苯酚,氯仿等试剂,也不需要乙醇沉淀
✔ 使用范围广:对细胞、细菌、动物组织提取均适用
✔ 操作简单快速:全程室温操作,10-20 分钟内可完成纯化步骤
✔ 提取纯度高:经过多次的柱吸附和洗涤,基因组 DNA 和蛋白质污染低
产品成分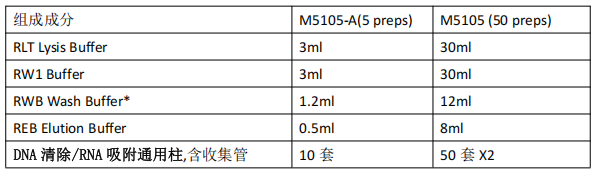
*首次使用前,在漂洗液 RWB Wash Buffer 中加入标签指定量的无水乙醇(5 preps/50 preps 分别加入 4.8 ml/48 ml 无水乙醇),充分混匀后使用,并做好标记。
*注意观察各溶液是否有析出或浑浊(尤其冬季低温环境时),可 37℃温浴复溶至溶液澄清, 避免影响使用效果。
运输和保存方式
常温运输,室温避光保存,有效期 12 个月。2-4°C 可保存更长时间
操作步骤
准备试剂(自备):无水乙醇,70%乙醇(RNase-free H2O 配制),TE buffer,1.5 ml RNase-free 离心管,台式离心机等。
一. 各种材料样本的准备处理
(a)贴壁培养的细胞:
移除培养基,用 PBS 清洗一次,在培养板中直接加入 350ul(<3X106 细胞 )或 600ul (3X106-6X106细胞)裂解液 RLT Lysis Buffer,水平放置片刻,便于裂解液均匀分布细胞表面 裂解,再使用移液器吹打细胞并移至收集管中,用力反复吹打 10 次,充分裂解直到看不到细胞 团为止,然后进行步骤 2。
注意:(1)对于 T 细胞/B 细胞等体积很小,RNA 含量低的细胞,建议增加细胞数量。
(2)不方便直接裂解的培养容器,可以使用细胞刮子刮下细胞或者胰蛋白酶消化后,将细胞收集到离心管中。
(b)悬浮培养细胞:
将悬浮培养的细胞和培养基一起移入离心管中,离心收集细胞,加入 350ul(<3X106 细胞 )或 600ul (3X106-6X106细胞)裂解液 RLT Lysis Buffer,用力反复吹打 10 次,充分裂解直到看不到细胞团为止,然后进行步骤二。
(c) 细菌细胞:
5000rpm 离心 3min 收集适量的菌体(<5x108),弃去上清,彻底移除培养基,加入 100ul 含有溶菌酶的 TE buffer(10mM Tris-HCl,1mM EDTA ,pH8.0),用移液器吹打混匀,室温静置孵育数分钟。加入 500ul 裂解液 RLT Lysis Buffer,剧烈振荡。如果有可见不溶物,12,000rpm 离心 5min,取上清,然后进行步骤二。
注意:革兰氏阴性细菌和革兰氏阳性细菌需要不同数量的溶菌酶和孵育时间,具体如下表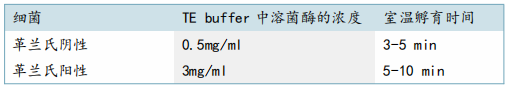
(d)动物组织:(适合内脏组织,肿瘤组织等,不适合皮肤等坚硬组织)
(1)匀浆器匀浆:新鲜组织加入 350ul(<15mg 组织)或者 600ul(15-30mg 组织)的裂解液 RLT Lysis Buffer,然后用玻璃匀浆器或者电动匀浆器将组织彻底匀浆,12,000rpm 离 心 5min,取上清,然后进行步骤 2
(2)液氮研磨:在液氮中将新鲜或-70℃冷冻的动物组织充分减碎研磨,将研磨成粉状 的样品转移至离心管中,加入 350ul(<15mg 组织)或者 600ul(15-30mg 组织)的裂解液 RLT Lysis Buffer,剧烈振荡 20 秒,12,000rpm 离心 5min,取上清,然后进行步骤二。
二.RNA 提取
1. 将处理好的匀浆液加到 DNA 清除/RNA 吸附通用柱上,12,000rpm 离心 1min,收集含有 RNA 的滤液。
注意:此步骤 RNA 存在滤液中,不可丢弃。
2. 较精确估计裂解液体积,加入等体积的 70%乙醇(RNase-free H2O 配制)到上述裂解液中(步骤 1 处理的样品),轻柔吹打混合均匀。
注意:加入 70%乙醇可能出现沉淀,正常现象,不影响提取过程,继续后续操作。
3. 立即将上述混合物加入新的 DNA 清除/RNA 吸附通用柱中(每次小于 800ul,若是体积过多, 可以分 2 次加入),12,000rpm 离心 30sec,弃掉废液。
4. 向 DNA 清除/RNA 吸附通用柱中加入 500ul 去蛋白液 RW1 Buffer,12,000rpm 离心 30sec, 弃掉废液。
5. 向 DNA 清除/RNA 吸附通用柱中加入 500ul 漂洗液 RWB Wash Buffer(使用前请先检查是否 已经加入指定体积的无水乙醇),12,000rpm 离心 30sec,弃掉废液。
6. 重复操作步骤 5
7. 将 DNA 清除/RNA 吸附通用柱放入收集管中,12,000rpm 离心 2min,尽量除去漂洗液。
8. 取出 DNA 清除/RNA 吸附通用柱,放入一个 RNase-free 的 1.5ml 离心管中,加入 25-50ul 的 洗脱液 REB Elution Buffer(或者 RNase-free H2O),室温静置 1min, 12,000rpm 离心 1min 获得 RNA 溶液。样品保存于-70℃,以备长期使用。
注意:加洗脱缓冲液不应少于 25ul,否则会影响回收率;为了获得更大浓度的 RNA,将离心的 RNA 溶液重新加入到吸附柱,重复洗脱一遍。
注意事项
1. 预防 RNase 污染,降解 RNA,
(a) 使用无 RNase 的塑料制品和枪头
(b) 操作时要戴一次性口罩和手套,实验过程中要勤换手套。
(c) RNA 在裂解液 RLT Lysis Buffer 中不会被 RNase 降解,但是提取实验后续处理过程中应 使用不含 Rnase 的塑料和玻璃器皿
(d) 配置溶液应使用无 RNase 的水。
2. RNA 提取过程必须在室温下进行,不可放置于冰上(直至洗脱离心后获得 RNA 方可放置于冰上),以避免中间产生不溶物堵塞离心柱。如果在开始离心时候,离心柱就被堵塞,可能是样 品含量过多或未完全裂解,导致吸附膜被堵塞,解决方案如下:
(a) 减少样品的体积
(b) 提高离心力
(c) 增加 RLT Lysis Buffer 用量
(d) 上柱前,12,000rpm 离心 5min,取上清,特别是匀浆的动植物组织,避免将组织碎片带入。
3. 加入 RLT Lysis Buffer 后,一定要充分振荡,保证 RNA 提取的效果;如果混合液非常粘稠难以转移,明显样品量过多,增加 RLT Lysis Buffer 用量。
4. 过基因组去除柱之后的细胞或组织裂解产物,上柱前需要加入等体积的 70%乙醇,充分混匀 之后加入离心柱离心。
5. 使用的样本避免反复冻融,以免影响 RNA 的产率和质量。
6. 关于 DNA 微量残留:一般情况下,总 RNA 提取过程中无法完全避免基因组 DNA 的微量残留。 使用本试剂盒,由于结合了独特的缓冲液体系和特殊吸附能力的吸附膜,获得的总 RNA 中,DNA 残留量比较少(一般通过电泳 EB 染色条件下是不可见的),对于大多数 RT-PCR 扩增过程是影 响不大的。如果实验对基因组 DNA 比较敏感,我们建议可以在以下情况下改善的
(a)后续可以使用 DNase I 酶经行处理,消化基因组 DNA
(b)选用跨内含子的引物,避免 mRNA 连接区,这样 DNA 就不能作为模板参与扩增反应
(c)选择基因组 DNA 和 cDNA 上扩增的产物大小不一样的引物对。
7. OD260/OD280和 OD260/OD230比值是衡量 RNA 纯度的指标,高质量的 RNA,OD260/OD280的值在 1.9-2.2 之间,OD260/OD230大于 1.8(比较纯净的比值大于 2.0)。如果 OD260/OD280比值过低,说明样品未完全裂解或匀浆不足,解决方案如下:
(a)改变匀浆方式
(b)减少样品的体积
(c)增加 RLT Lysis Buffer 裂解液的使用量
(d)OD260/OD280受到测定溶液的 pH 值影响,同一个 RNA 样品,假设在 10mM Tris,pH7.5 溶 液中测定的 OD260/OD280值 1.8-2.1 之间,在水溶液中测定的值可能在 1.5-1.8 之间,但是这个不 表示 RNA 不纯。
8. 裂解液 RLT Lysis Buffer 和去蛋白液 RW1 Buffer 中含有刺激性化合物,操作时要带乳胶手套, 避免沾染皮肤,眼睛或衣服等,若沾染皮肤,眼睛时,请用大量的清水或者生理盐水冲洗干净。